A vacinação é uma das estratégias mais eficazes para a prevenção de infecções. Simplificando, a ação da vacina pode ser explicada como forma de antecipar o contato do corpo com o microrganismo infectante ou parte dele de maneira segura, visando a estimular e preparar o sistema imunológico para quando de fato for desafiado no contato com o agente causador da doença.
Em 1796, o médico inglês Edward Jenner (1749-1823) criou a primeira vacina do mundo a partir da observação de que pessoas que contraíram a varíola bovina (cowpox) estariam protegidas da infecção pela varíola humana, uma doença viral frequentemente mortal. Jenner deu a esse processo o nome de vacinação.
Após quase dois séculos do desenvolvimento da primeira vacina, em 1980, a Organização Mundial da Saúde (OMS) declarou oficialmente: “O mundo e todos os seus povos estão livres da varíola”. A afirmação marcou o fim de uma doença que atormentou a humanidade por pelo menos três mil anos, matando 300 milhões de pessoas somente no século 20. Ainda hoje, a erradicação da varíola é considerada a maior vitória da medicina moderna, sendo lembrada com esperança na luta para eliminar doenças infecciosas.
Cabe insistir que vacina não é um gasto, é um investimento em saúde. Segundo a OMS, existem vacinas para prevenir mais de 20 doenças fatais. A imunização atualmente previne de 2 a 3 milhões de mortes todos os anos por doenças como pneumonia, meningite, hepatite e sarampo.
Mundialmente reconhecido, o Programa Nacional de Imunização (PNI) brasileiro, criado em 1973, é considerado referência pela Organização Pan-americana da Saúde (Opas). Parte do Sistema Único de Saúde (SUS), o PNI oferece gratuitamente todas as vacinas recomendadas pela OMS. Além de distribuir 25 tipos de vacinas, o país ainda produz e exporta várias delas para mais de 70 países. Atualmente, são disponibilizados gratuitamente pela rede pública de saúde cerca de 300 milhões de doses de imunobiológicos, para combater mais de 19 doenças, em diversas faixas etárias.
Na linha de frente do fornecimento, estão os laboratórios públicos produtores de vacinas. Atendendo às rigorosas exigências de produção e regulamentação, quase a totalidade das vacinas entregues pelo PNI é produzida nacionalmente. Alavancando o desenvolvimento, estão os acordos de transferências de tecnologia em parcerias público-privadas. Os laboratórios públicos e respectivas vacinas estão destacados na figura 1.

BIO-MANGUINHOS
• febre amarela
• poliomielite oral atenuada
• poliomielite inativada
• tríplice viral
• tetra viral
• rotavírus
• meningite AC
• Haemophillus influenzae B (Hib)
• peneumocócica

BUTANTAN
• influenza
• raiva uso humano
• DTP, DT, dT, DTPa
• hepatite A
• hepatite B
• HPV

TECPAR
• raiva uso veterinário

FAP
• BCG

BIO-MANGUINHOS
• febre amarela
• poliomielite oral atenuada
• poliomielite inativada
• tríplice viral
• tetra viral
• rotavírus
• meningite AC
• Haemophillus influenzae B (Hib)
• peneumocócica

BUTANTAN
• influenza
• raiva uso humano
• DTP, DT, dT, DTPa
• hepatite A
• hepatite B
• HPV

TECPAR
• raiva uso veterinário

FAP
• BCG
Normalmente, o processo de desenvolvimento de vacinas leva anos, passando pelas etapas iniciais de testes laboratoriais e pré-clínicos em animais, seguido pelas fases de testes clínicos para comprovar a segurança, imunogenicidade (capacidade de provocar uma resposta imune) e eficácia.
Na rotina de produção de vacinas humanas, exigências regulatórias e de processos devem ser rigorosamente cumpridas. A Certificação nas Boas Práticas de Fabricação (BPF) de medicamentos é obrigatória. O atendimento às BPF, reguladas pela Agência Nacional de Vigilância Sanitária (Anvisa) em 2019, define diretrizes mínimas, visando garantir que os medicamentos sejam consistentemente produzidos e controlados de acordo com padrões de qualidade previamente estabelecidos.
Periodicamente, os produtores são inspecionados pela Anvisa e, no caso de exportação, o laboratório que fabrica os medicamentos também deve ser pré-qualificado pela OMS. Áreas limpas certificadas, equipamentos qualificados, processos validados, insumos aprovados e operadores devidamente paramentados e treinados são requisitos mínimos para a produção.
As áreas de produção, conhecidas como salas limpas, devem ser projetadas e construídas de forma a minimizar os riscos de contaminação. Todo detalhe é importante, desde a infraestrutura construída com materiais resistentes, como aço inox e pintura epóxi, cantos arredondados e de superfícies lisas de fácil limpeza, sem geração de partículas, até os sistemas de ar passando por filtros de alta eficiência, controle de temperatura, umidade e pressão. Os equipamentos e mobiliários devem ser construídos com materiais resistentes às rotinas frequentes de desinfecção do ambiente (figura 2).

As vacinas recomendadas mundialmente são classificadas em quatro tipos: atenuada, inativada, de subunidades e toxoide. Essa classificação depende do tipo do antígeno – princípio ativo, insumo farmacêutico ativo (IFA) – usado na fabricação. As primeiras são produzidas com microrganismos atenuados, que são enfraquecidos e incapazes de causar a doença. As vacinas inativadas são fabricadas com o agente inerte, incapaz de fazer o ciclo infeccioso, mas capaz de estimular o sistema imune. As vacinas de subunidades são produzidas com pequenos pedaços, como proteínas ou polissacarídeos, sintéticos ou purificados a partir do próprio microrganismo. A vacina de toxoide é especificamente fabricada com a toxina inativada (figura 3).


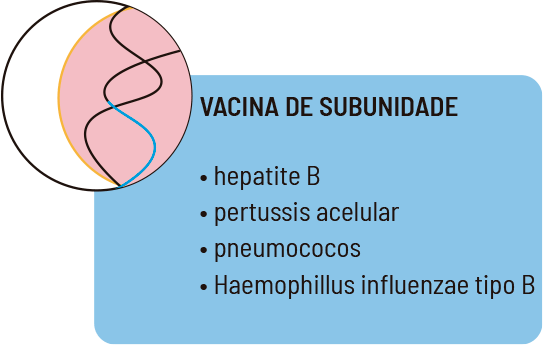
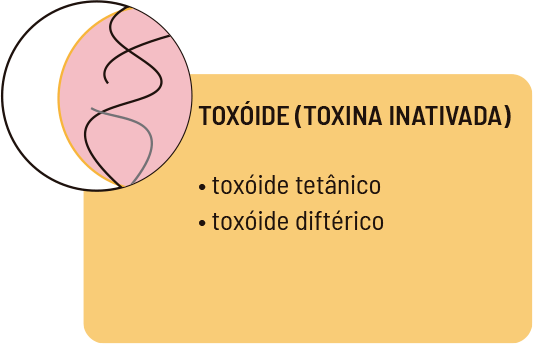
Com o avanço tecnológico, novas estratégias estão sendo utilizadas. Atualmente, na corrida para o desenvolvimento de vacinas para a covid-19, além da tradicional tecnologia com vírus inativados, já estão em testes clínicos avançados vacinas utilizando vetores – bactérias ou vírus clonados com fragmentos específicos de material genético responsável pela produção dos antígenos –, assim como vacinas formuladas com o material genético (DNA ou RNA) do microrganismo (figura 4).


O processo de produção é composto por várias etapas, como mostra figura 5. Resumidamente, inicia com a produção do IFA e segue com a formulação e etapas do processamento final (envase, liofilização, recravação, rotulagem e embalagem final).

As vacinas podem ser apresentadas na forma farmacêutica líquida ou em pó, liofilizadas (desidratas) ou não. Além da apresentação, podem variar o número de doses e a via de administração (oral, subcutânea, intramuscular e intradérmica), que são definidas no desenvolvimento do produto.
A tecnologia de produção da vacina é ligada especialmente ao tipo de IFA utilizado. Basicamente, as etapas de obtenção do IFA consistem na obtenção propriamente dita do antígeno, purificação, conjugação (ligação com proteína, caso aplicável) e estabilização.
Existem diversos substratos e plataformas tecnológicas de produção de vacinas. Na figura 6, são ilustrados exemplos de vacinas com seus respectivos substratos e plataformas tecnológicas.


Para a produção de vírus, é fundamental a disponibilidade de células in vivo ou in vitro. Por exemplo, nas vacinas da febre amarela e da gripe, ovos com embriões de galinha são utilizados como verdadeiras fábricas de vírus. Os ovos são inoculados diretamente com vírus atenuados. No sistema in vivo, as células dos tecidos vivos fabricam as partículas virais sem grandes exigências nutricionais, sem serem necessárioas, de modo geral, condições ambientais de temperatura e umidade ideais à manutenção das células. A figura 7 mostra resumidamente o processo de produção do IFA da vacina de febre amarela.
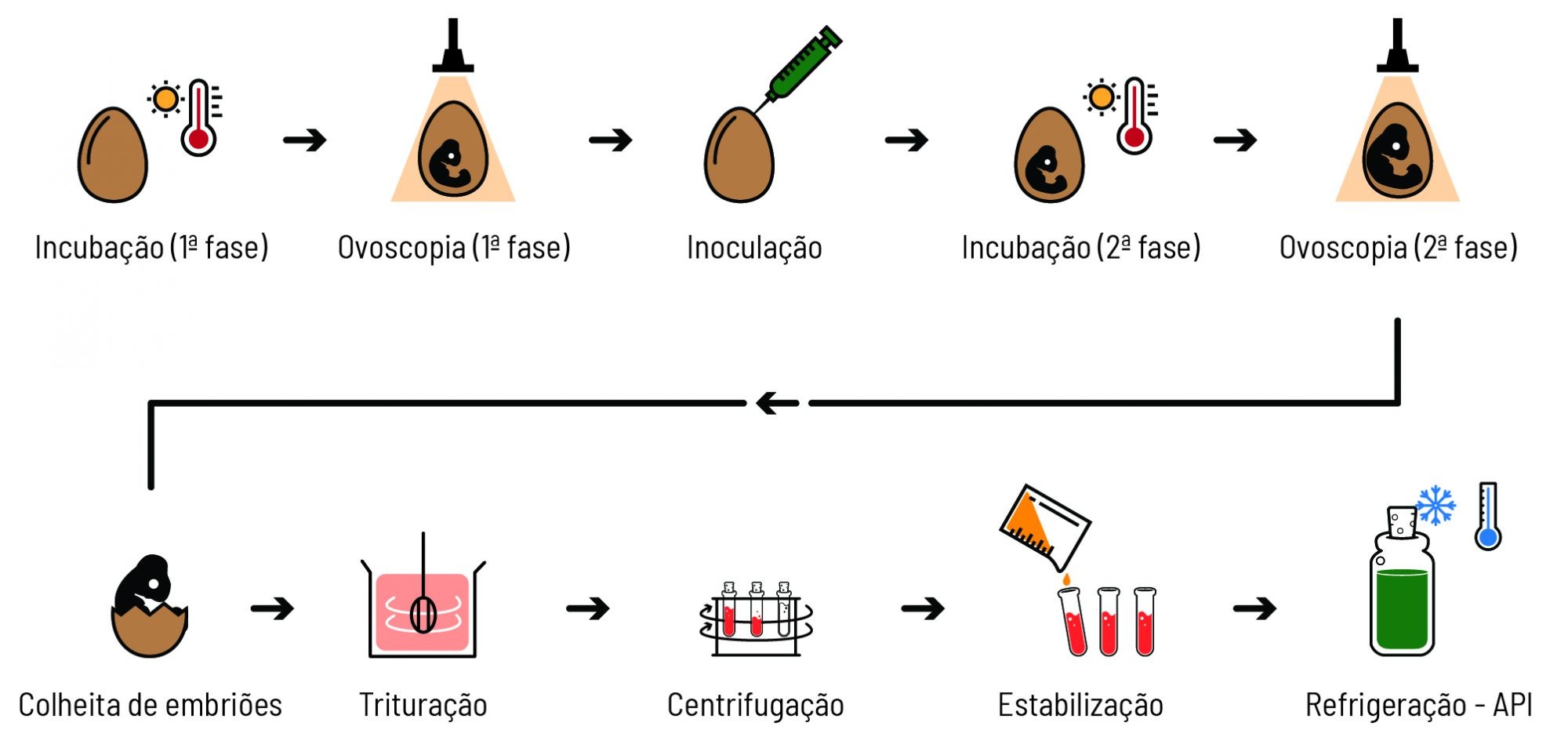
No cultivo in vitro, as células aderentes ou não, em sistemas do tipo garrafas rollers, cell factory e biorreatores de grande escala, dependem do fornecimento das necessidades nutricionais externas, além das condições ambientais, como na produção das vacinas de rotavírus e na tríplice viral. Dependendo do vírus e do tipo celular, as partículas virais são liberadas espontaneamente ou de forma forçada no sobrenadante (fração líquida). A purificação viral é comumente realizada por centrifugação ou filtração.
Bactérias podem ser cultivadas in vitro em reatores ou fermentadores, visando à produção de massa celular, no caso da utilização da célula bacteriana inteira, purificada, como o componente celular da coqueluche, ou de partes da célula bacteriana, como as vacinas meningocócicas ou pneumocócicas, constituídas dos polissacarídeos da cápsula bacteriana. Em outros casos, o antígeno pode ser o produto do metabolismo da célula bacteriana, como as toxinas tetânicas e diftéricas, que são inativadas, gerando os toxoides (componentes não tóxicos estimulantes do sistema imunológico).
Por vezes, o cultivo de bactérias patogênicas encarece demasiadamente o processo, pois em geral exigem nutrientes e condições para crescimento dispendiosos. Já é possível obter antígenos a partir de células recombinantes, como é o caso da toxina diftérica.
Nas vacinas bacterianas de subunidades, por exemplo, quando se trata de um antígeno polissacarídico, é ainda necessária a conjugação com uma proteína carreadora, pois os polissacarídeos sozinhos não são capazes de induzir uma resposta de memória duradoura. Assim, os toxoides tetânico e diftérico são utilizados em uma reação química, na qual se ligam aos antígenos polissacarídicos. Há várias vacinas disponíveis obtidas dessa maneira, como a do Haemophilus influenzae tipo b conjugada, ou a pneumocócica (figura 8).
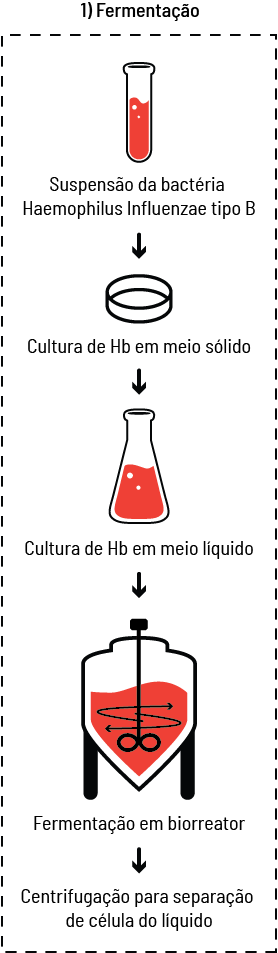

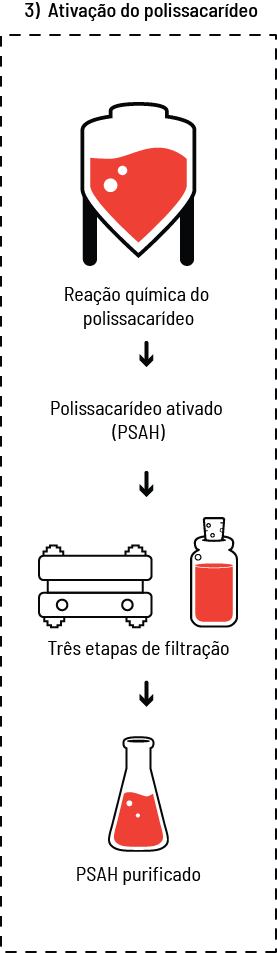
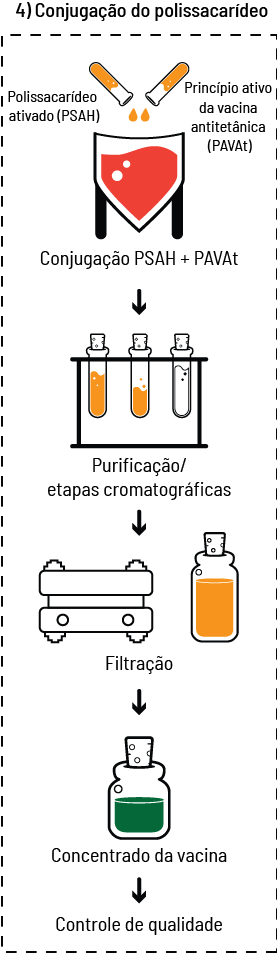
O processo de expansão das células bacterianas ocorre em reatores ou fermentadores, que são sistemas fechados, contendo meios de cultivo apropriados para a bactéria que se deseja cultivar, com sistema de aeração, homogeneização, controle do pH (grau de acidez) e metabólitos, criando dessa forma um ambiente propício para a proliferação bacteriana. A partir da obtenção da massa celular, inicia-se o processo de purificação do antígeno.
Atualmente, cada vez mais, lança-se mão das técnicas de cromatografia, como gel filtração ou peneira molecular, troca iônica, afinidade, entre outras. Conta-se também com métodos de ultrafiltração, tanto para separação de espécimes moleculares quanto para concentração do IFA.
Durante todas as etapas da produção, os riscos são gerenciados e testes de controle são realizados. Avaliam-se parâmetros como esterilidade, potência da vacina, avaliação da pureza, condições de conjugação, detecção e determinação da concentração de resíduos da purificação.
No processo de garantia da qualidade, analisam-se todos os dados de produção, resultados de controle da qualidade, parâmetros ambientais das salas limpas, dados de rendimentos e perdas, consistência de produção, além do monitoramento dos operadores. Há uma sinergia entre produção, controle e garantia da qualidade para que as vacinas sejam dadas como aprovadas.
Ampliar e consolidar a produção nacional de vacinas é um dos grandes desafios do Brasil, uma vez que se trata de um processo complexo e com muitas variáveis. As flutuações relacionadas a uma produção de imunobiológicos devem ter seus riscos mapeados e minimizados a fim de garantir o abastecimento do mercado.
No Brasil, um cenário bastante animador é a perspectiva da construção do Complexo Industrial de Biotecnologia em Saúde em Santa Cruz (RJ), o qual produzirá anualmente até 120 milhões de frascos, passando ser a maior fábrica de vacinas da América Latina. Além de novas plantas fabris, deve-se investir em adequar as fábricas já existentes dos laboratórios públicos para assim contemplar as crescentes demandas regulatórias nacionais e internacionais, mantendo o abastecimento atual.
A incorporação tecnológica e o desenvolvimento de novas vacinas também devem ser priorizados a fim de oferecer a população o que há de melhor. No entanto, esses dois caminhos são considerados longos e complexos, nos quais se têm um alto investimento e retorno em longo prazo, o que faz com que nem sempre sejam privilegiados. Porém, são esses os alicerces – junto com as produções já consolidadas – necessários para evitar ou minimizar o risco de desabastecimento de vacinas em momentos de demanda mundial.
Deve-se ter especial atenção ainda ao processo logístico envolvido na viabilização da produção de vacinas, uma vez que boa parte dos insumos e equipamentos utilizados é importada, demandando a facilitação e priorização desses processos altamente estratégicos.
Outro fator importante diz respeito à formação, retenção e valorização da mão de obra qualificada e especializada. Normalmente, esses recursos humanos têm sua formação refinada dentro do próprio complexo industrial, já que receberam conhecimento específico – e muitas vezes sigiloso – na própria instituição. Entretanto, nos laboratórios públicos, a realidade é outra: enfrentam-se dificuldades para contratar, formar e reter talentos, gerando uma lacuna nesses ambientes.
Com a atuação nas frentes descritas acima, teremos ainda que equacionar a decrescente adesão ao PNI. Falta de conhecimento sobre doenças consideradas erradicadas, falsas notícias (fake news) e horários limitados das salas de vacinação são fatores que estão contribuindo com as baixas coberturas vacinais.
Infelizmente, movimentos antivacinas ganham espaço. Diversos estudos demonstram a eficácia e o papel relevante da introdução do uso de vacinas na história, mas aqueles que se recusam a vacinar fazem escolhas individuais que podem repercutir em toda a sociedade – doenças tidas como erradicadas podem retornar, como o caso do sarampo.
A onda do antivacinismo pode estar relacionada ao questionamento da segurança das vacinas, ao receio de seus efeitos colaterais, ou mesmo à crença de que as pessoas não são vulneráveis a essas doenças. Assim como qualquer medicamento, as vacinas podem gerar efeitos adversos. Mas, ao aprovar seu uso, entende-se que seus benefícios superam o risco da ocorrência de tal evento, uma vez que a doença traria consequências muito mais graves. Acredita-se que a comunicação de qualidade e transparência sobre as vacinas seria o melhor instrumento para lidar com tais movimentos.
Com a globalização e a situação que atualmente vivemos com a pandemia do covid-19, realmente lidar com esses gargalos citados e impulsionar as iniciativas de consolidação da produção nacional de vacinas e cobertura vacinal é o caminho para o sucesso e a esperança de dias melhores.
Carla França Wolanski de Almeida
Vice-Diretoria de Produção, Fiocruz
Caroline Moura Ramirez
Gestão integrada de Projeto de Transferência de Tecnologia e Produção da Vacina Covid-19, Fiocruz
Wania Renata dos Santos
Departamento de Vacinas Virais, Fiocruz

Sistemas que combinam árvores nativas com cultivo de cacau em pequena escala protegem uma alta diversidade de aves no sul da Bahia, mas espécies que se alimentam de frutos e insetos são negativamente afetadas, segundo estudo que reforça a importância de se conservar a vegetação original do bioma.

Mais um tradicional embate entre mim e Noel. Desta vez, o ‘simpático’ barbudo não trouxe um presente, mas, sim, um problema interessante: será possível pintar os números de 1 a 9 usando duas cores apenas, evitando que um deles seja a média dos outros dois?

Coordenadora-geral da Olimpíada Nacional em História do Brasil, a professora da Unicamp Cris Meneguello conta como nem a covid-19 atrapalhou a realização da 12ª edição da competição, que, baseada em documentos, leitura e análise crítica de fontes, proporciona uma visão mais ampla do país .
Doença causada pelo parasita Toxoplasma gondii atinge milhões de brasileiros, com consequências graves para a saúde pública. Pesquisadores estão propondo alternativas de tratamento para acelerar o processo de descoberta de novos medicamentos e assim beneficiar os pacientes.

A exploração do espaço voltou a ganhar momento, com a entrada em cena não só de novas agências espaciais, mas também de empresas que exploram comercialmente essa atividade. A tensão ideológica que marcou esse campo foi substituída pela cooperação

O mercado de sementes modificadas e dependentes de pesticidas tóxicos à saúde e ao ambiente está cada vez mais concentrado em algumas poucas megaempresas. É essencial visibilizar as formas de produção por trás do que comemos para alcançar alternativas saudáveis e justas

Há 50 anos, o lançamento do satélite Landsat-1 transformou nosso olhar sobre a superfície terrestre. Hoje, as técnicas de machine learning e deep learning promovem uma nova revolução, desta vez na “visão” dos computadores e no sensoriamento remoto do planeta

A pele – maior órgão do corpo humano – é habitada por uma vasta e diversa comunidade de micro-organismos, a microbiota. Esses seres invisíveis não só nos protegem contra doenças e alergias, mas também afetam nosso odor corporal, tornando-nos mais (ou menos) atraentes para insetos.

Há cerca de mil anos, a explosão de uma estrela no céu revelou pela primeira vez a luz síncrotron, radiação emitida por partículas elétricas e ultravelozes. Hoje, essa luz – agora gerada por aceleradores, como o Sirius, no Brasil – é uma ferramenta importante da ciência

As atividades de mineração da empresa Braskem em Maceió (AL) causaram o afundamento do solo, o que fez com que cerca de 60 mil pessoas tivessem que deixar suas casas. Essa população de deslocados internos ambientais ainda espera por compensações

Gases nobres são ditos inertes por não reagirem com outros elementos. Porém, depois de mais de um século de pesquisa, a química avançou na compreensão das condições com que esses elementos formam compostos. Hoje, vários derivados deles são conhecidos na Terra e no espaço.

Em um mundo que pede por soluções sustentáveis, a microbiologia tem papel importante: o uso de microrganismos para a fabricação de bioprodutos ‘verdes’. Planta-piloto em uma universidade brasileira promete impulsionar de forma pioneira a área no país
| Cookie | Duração | Descrição |
|---|---|---|
| cookielawinfo-checkbox-analytics | 11 months | This cookie is set by GDPR Cookie Consent plugin. The cookie is used to store the user consent for the cookies in the category "Analytics". |
| cookielawinfo-checkbox-functional | 11 months | The cookie is set by GDPR cookie consent to record the user consent for the cookies in the category "Functional". |
| cookielawinfo-checkbox-necessary | 11 months | This cookie is set by GDPR Cookie Consent plugin. The cookies is used to store the user consent for the cookies in the category "Necessary". |
| cookielawinfo-checkbox-others | 11 months | This cookie is set by GDPR Cookie Consent plugin. The cookie is used to store the user consent for the cookies in the category "Other. |
| cookielawinfo-checkbox-performance | 11 months | This cookie is set by GDPR Cookie Consent plugin. The cookie is used to store the user consent for the cookies in the category "Performance". |
| viewed_cookie_policy | 11 months | The cookie is set by the GDPR Cookie Consent plugin and is used to store whether or not user has consented to the use of cookies. It does not store any personal data. |
