O metanol tornou-se o vilão nos noticiários devido ao seu uso na adulteração de bebidas alcoólicas. Compreender como esta substância atua no organismo humano gerando efeitos tóxicos é uma oportunidade de se discutir vários tópicos em química, tais como as reações ácido-base, a oxidação de álcoois e a variação do número de oxidação.
O texto publicado na seção “Pequenas perguntas, grandes questões” da CH 426, intitulado “Metanol, ácido fórmico e bicarbonato de sódio: como o equilíbrio químico entra em ação?”, apresenta o problema da metabolização do metanol que leva à formação do ácido fórmico e à consequente acidificação do sangue. A dica de Química deste mês discute as etapas de oxidação do metanol no organismo.
A adição do metanol em bebidas alcoólicas traz inúmeros efeitos tóxicos ao organismo humano. Isso se deve à metabolização deste álcool primário que, por ação enzimática, produz aldeído fórmico e ácido fórmico. Em etapas mais lentas, o ácido fórmico pode ser convertido em seu formiato e ser decomposto em gás carbônico e água. Porém, a formação do ácido fórmico por si só leva a inúmeros efeitos deletérios ao organismo, como a acidose metabólica, lesão do nervo óptico, danos no sistema nervoso central, dentre outros.
Nossa dica de química dá ênfase ao processo de metabolização do metanol no organismo, que é um processo que envolve a oxidação do carbono alfa, ou seja, aquele ligado diretamente ao grupo OH do álcool (Figura 1) através do sistema enzimático.
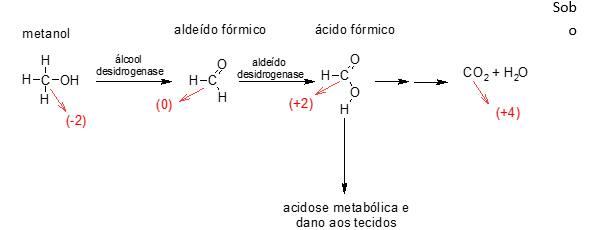
Sob o tema oxidação de álcoois, o professor pode iniciar a aula com a seguinte pergunta para a turma: “Por que o metanol, um álcool utilizado na adulteração de bebidas, faz mal à saúde humana?”. As respostas dos alunos devem ser ouvidas e, a partir dessa discussão inicial, o processo de metabolização do metanol pelo organismo humano pode ser apresentado. Contudo, os números de oxidação (nox) devem ser omitidos se a turma tiver conhecimentos para calcular os nox do carbono do metanol e dos produtos de oxidação (aldeído fórmico, ácido fórmico e gás carbônico). O professor deve solicitar esse cálculo por parte da turma. Ao finalizarem seus apontamentos, o cálculo deve ser feito com toda a turma para a verificação dos resultados.
Em seguida, o professor deve perguntar à turma qual das espécies deve ser a mais ácida. Se o conhecimento sobre a força dos ácidos em função de seus pKa (logaritmo negativo da constante de acidez) for um conteúdo dado, este pode ser utilizado para se fazer inferências quanto à espécie mais ácida. Neste caso é o ácido fórmico (pKa 3,75 a 25°C). Mas os estudantes podem intuitivamente apontar o ácido fórmico, e cabe ao professor explorar os efeitos eletrônicos da carboxila do ácido que favorecem a sua acidez.
Por fim, os danos decorrentes da presença do ácido fórmico no organismo devem ser apresentados, respondendo, assim, à pergunta inicial. Dando prosseguimento ao tema, o texto publicado em CH 426 pode ser fornecido à turma para que os estudantes justifiquem o uso do bicarbonato de sódio para combater os efeitos da acidose no sangue, apresentando a reação ácido-base correspondente.
Por que o metanol é tão tóxico? Boletim eletrônico da SBQ, nº 1668 – 02/10/2025. Disponível em: https://boletim.sbq.org.br/noticias/2025/n4300.php. Acesso em novembro de 2025.