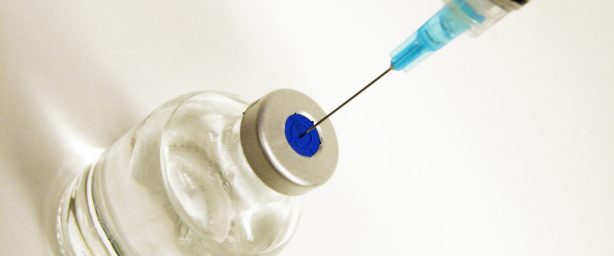
A primeira vacina 100% brasileira contra o HIV, o vírus causador da Aids, será testada em macacos ainda este ano e, se obtiver sucesso, poderá em alguns anos ser empregada em ensaios com humanos. Chamada HIVBr18, a vacina foi desenvolvida por pesquisadores do Instituto do Coração da Faculdade de Medicina da Universidade de São Paulo (FMUSP) e a expectativa é que ela possa repetir nos macacos a eficácia dos testes em camundongos, quando foi capaz de aumentar a resposta imune contra componentes do vírus. Em humanos, espera-se que a HIVBr18 possa reduzir a carga viral, impedindo o desenvolvimento da Aids e mantendo o paciente saudável, como as drogas antirretrovirais fazem agora.
Os testes em macacos Rhesus, que serão realizados no Instituto Butantan, em São Paulo, têm o objetivo de determinar a melhor via de administração da vacina. Esses macacos apresentam, entre os modelos animais, o sistema imunológico mais parecido com o de humanos e, em tese, uma estratégia de vacinação bem-sucedida nesses macacos também seria satisfatória em nossa espécie.
“Além da versão original da vacina, vamos criar outras com diferentes vetores, como o adenovírus de chimpanzé e a vacina da febre amarela, e ver qual gera a melhor resposta imune”, diz o médico Edecio Cunha Neto, coordenador da pesquisa e chefe do Laboratório de Imunologia Clínica e Alergia da FMUSP.
Longo caminho
A pesquisa, iniciada em 2001, tinha como objetivo identificar por que determinados indivíduos infectados com HIV por 10 anos ou mais não desenvolvem Aids. Os progressores lentos, como essas pessoas são chamadas, costumam manter altos níveis de linfócitos T CD4, embora essas células do sistema imune sejam o alvo do vírus.
A quantidade desses linfócitos no sangue indica quão debilitado um paciente está: a Aids é definida pela presença de um volume menor que 200 dessas células por milímetro cúbico de sangue. “Queríamos saber se os progressores lentos brasileiros tinham características em comum com os de outros países, como ter um subtipo de linfócito que ataca células infectadas pelo vírus, como outros T CD4 e macrófagos”, explica.
Cunha Neto e sua equipe selecionaram, entre os vírus que circulavam nesses pacientes, 18 fragmentos de oito das nove proteínas do HIV que são conservados evolutivamente, ou seja, são essenciais para a multiplicação do vírus, e que deveriam ser reconhecidos pelo sistema imune da maioria dos soropositivos. Eles testaram essa hipótese apresentando os fragmentos para reconhecimento pelo sistema imunológico de pacientes infectados com HIV. Ao serem reconhecidos, esses pedaços de proteína disparam a produção de interferon gama, sinal que os pesquisadores mediram.

- A vacina da USP foi feita com base em fragmentos do HIV que circulava em soropositivos chamados progressores lentos, indivíduos infectados há mais de 10 anos, mas que não desenvolvem a doença. Após testarem os fragmentos em culturas de células dos pacientes e constatarem alta resposta imunológica, os cientistas criaram uma vacina de DNA que foi aplicada em camundongos comuns e transgênicos, obtendo bons resultados. (ilustração: Luiz Baltar)
Os pesquisadores verificaram que mais de 90% dos pacientes infectados com HIV – incluindo os que já desenvolveram Aids – apresentaram respostas imunes aos 18 fragmentos. “Para nossa surpresa, vimos uma grande resposta imunológica não só dos progressores lentos, mas também de outros soropositivos, inclusive entre os já diagnosticados com Aids. Cerca de 90% reconheciam pelo menos um fragmento, e a média foi de cinco pedaços de proteína reconhecidos, o que é um grande número”, relata o médico.
Duplamente inovadora
Estimulados pelos bons resultados, os pesquisadores cogitaram a possibilidade de ter um protótipo de vacina nas mãos. Criaram então uma molécula circular de DNA (plasmídeo) que codificava esses fragmentos e a testaram em camundongos, nos quais observaram uma resposta para oito dos fragmentos. Eles partiram então para testes com quatro variedades de camundongos transgênicos que incorporam elementos do sistema imunológico humano importantes para a ativação dos linfócitos T CD4. “Todas as quatro linhagens desencadearam respostas imunes similares à dos camundongos originais”, afirma Cunha Neto.
Testes adicionais com uma nova versão da vacina, criada a partir de fragmentos conservados dos principais subtipos de HIV que circulam no mundo, também mostraram resultados positivos, especialmente quando a vacina foi adicionada a um vetor viral – as sequências de DNA foram colocadas na estrutura de um vírus, o que facilita sua entrada nas células. “Essa nova versão poderia gerar uma reação imunológica para a maior parte das variedades de HIV que existem, permitindo que a vacina fosse usada em diversos lugares do planeta”, observa o médico.

- Depois do sucesso dos testes em camundongos, a vacina será testada em macacos ‘Rhesus’, com o objetivo de determinar a melhor via de administração. (ilustração: Luiz Baltar)
Para o biólogo Marcelo Soares, coordenador do Laboratório de Virologia Humana da Universidade Federal do Rio de Janeiro (UFRJ), a vacina inova em dois pontos. Primeiro, na abordagem de múltiplos subtipos de HIV. “As estratégias de desenvolvimento de vacina costumam se concentrar em um ou dois subtipos e, em geral, nos que renderão mais para as empresas, como o B, comum nos Estados Unidos”, comenta Soares. Segundo, o uso de fragmentos de vírus circulantes em progressores lentos pode vir a identificar alguma deficiência do HIV ou característica útil com potencial terapêutico. “No futuro, talvez consigamos tornar progressores lentos todos os soropositivos”, sugere o biólogo.
Os testes iniciais com os Rhesus começarão ainda no segundo semestre, com a otimização dos vetores marcada para o início do ano que vem. Cunha Neto acredita que, se tudo der certo, testes clínicos de fase 1 em humanos poderão ser realizados daqui a dois anos. Se todas as etapas em humanos forem bem-sucedidas, uma vacina funcional pode estar pronta em 2019. “Isso vai depender de financiamento. Há a vantagem competitiva de a HIVBr18 ter sido desenvolvida aqui, mas ainda assim um teste clínico custa no mínimo US$ 100 milhões”, ressalta o médico.
Fred Furtado
Ciência Hoje/ RJ
Texto originalmente publicado na CH 307 (setembro de 2013).