Além das vacinas contra dengue já licenciadas, existem outras em estudo. Umas delas foi desenvolvida nos Institutos Nacionais de Saúde (NIH), nos Estados Unidos, em colaboração com o Instituto Butantã no Brasil, cujos estudos com voluntários humanos estão em fase final.
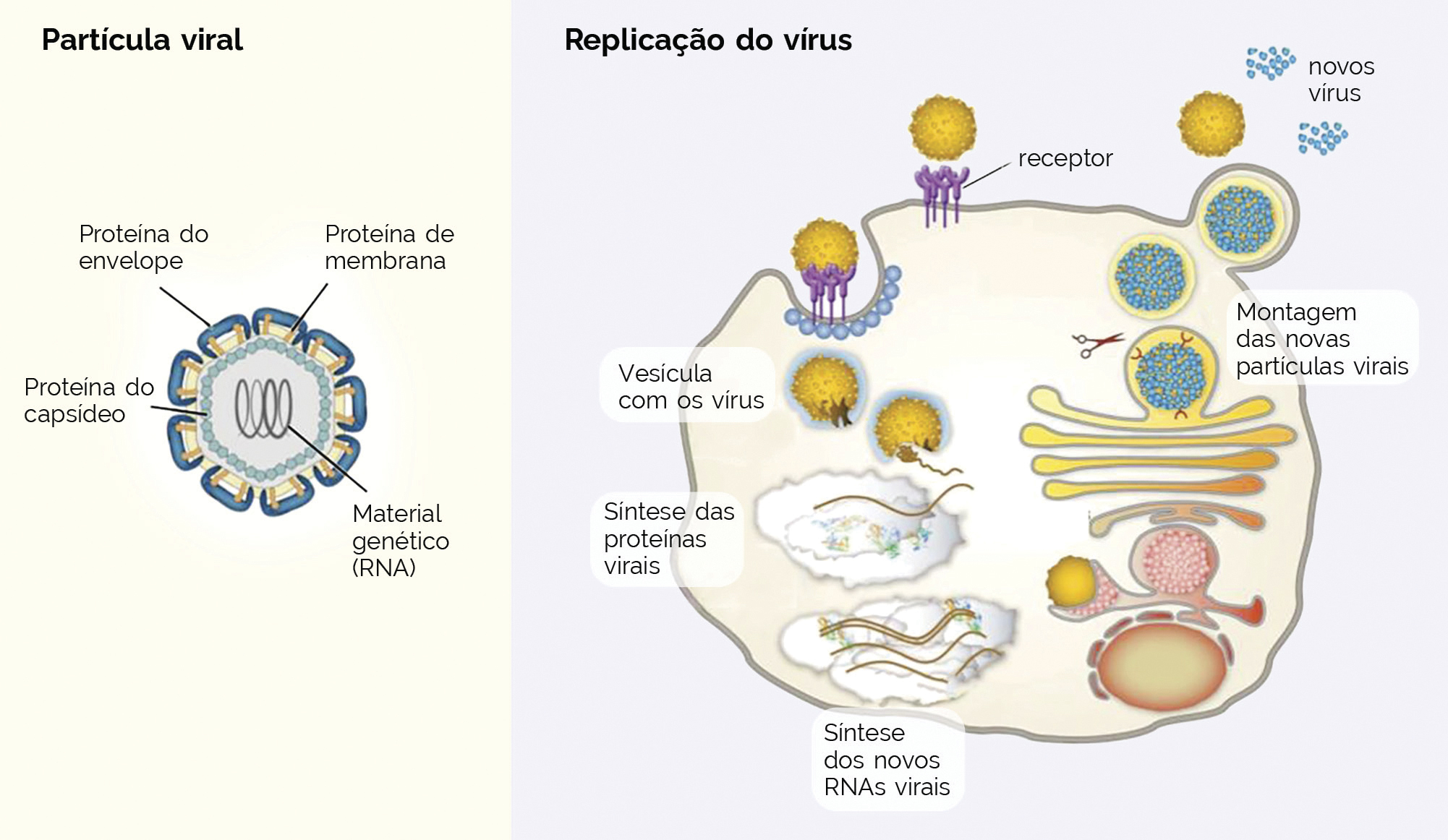
Esta vacina, também viva atenuada, é constituída dos DENV atenuados pelas técnicas de biologia molecular, em que os cientistas retiraram um pequeno pedaço do RNA do vírus. Isso fez com que tais vírus se tornassem atenuados, não causando mais a doença. Os vírus 1, 3 e 4 foram atenuados e o DENV 4 atenuado foi utilizado para a troca dos genes das proteínas M e E pelos mesmos genes de DENV 2.
Até o momento, não temos dados suficientes para saber se essa vacina será protetora contra os quatro sorotipos no Brasil, pois, como os sorotipos 3 e 4 de DENV não estão circulando muito no país há vários anos, a avaliação da proteção na população vacinada não pode ser estabelecida.
De qualquer modo, ainda existem muitas lacunas nos estudos das vacinas contra a dengue e novas estratégias vacinais são bem-vindas para auxiliar no combate a essa doença que aflige a nossa população quase todos os verões. Com esse objetivo, nosso grupo tem trabalhado com vacinas de DNA contra dengue há mais de duas décadas.
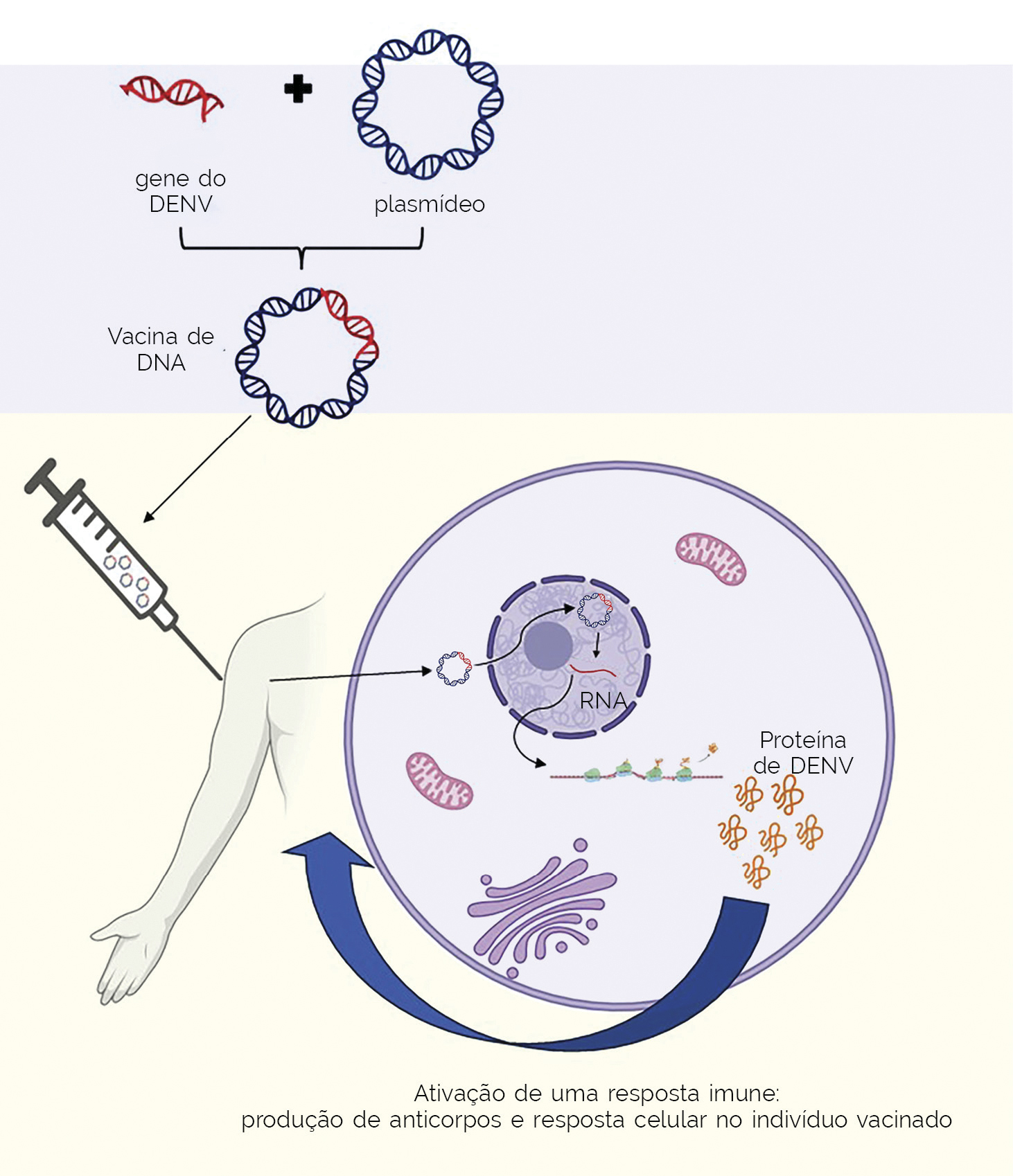
Tais vacinas são constituídas de pequenos DNAs circulares, chamados plasmídeos, que contêm um ou mais genes do vírus. Uma das vantagens das vacinas de ácidos nucleicos, como as de DNA ou de RNA, é que elas são capazes de ativar uma ampla resposta na pessoa vacinada, com a produção de anticorpos e de uma resposta imune celular, em que são ativadas células capazes de destruir outras células infectadas com o vírus.
Outra vantagem das vacinas de DNA é o baixo custo de produção em relação a outros tipos de vacina, sem a necessidade de armazenamento a baixas temperaturas, o que representa uma grande economia e vantagem para a sua utilização em um país continental como o Brasil (figura 3).