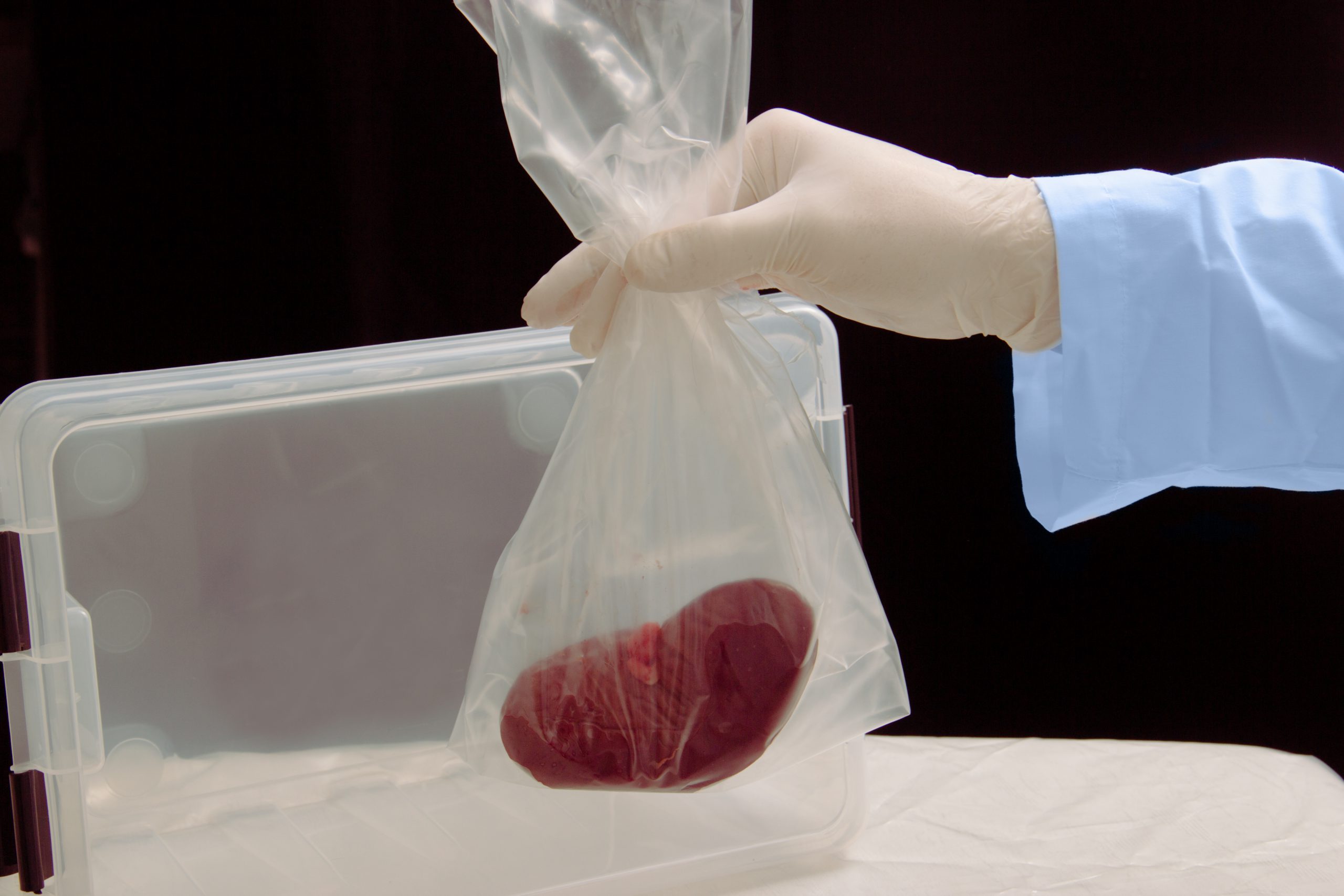
A série sul-coreana Round 6 lançou luz sobre o mercado de tráfico de órgãos humanos. Um sistema ético de distribuição de órgãos e o avanço do conhecimento científico são essenciais para que o transplante, fundamental para o tratamento de diversas doenças relacionadas à falência de órgãos, seja acessível a um número cada vez maior de pacientes.
CRÉDITO: A PARTIR DE FOTO ADOBE STOCK